在生命科学的浩瀚星空中,RNA正成为继蛋白质之后,全球药物研发的下一片蓝海。近日,寻鲸生科两位创始人——清华大学张强锋教授与北京大学汪阳明教授强强联手,在国际顶级学术期刊Nature Biotechnology上发表了最新研究成果Predicting small molecule–RNA interactions without RNA tertiary structures。(原文链接 : https://www.nature.com/articles/s41587-025-02942-z)。这一突破不仅展示了人工智能在靶向RNA药物筛选领域的巨大潜力,更标志着寻鲸生科在“AI驱动RNA药物研发”道路上迈出了坚实的一步。
近年来,研究发现RNA也像蛋白质一样能折叠成精巧的三维结构,并与小分子结合实现精准识别,从而调控关键生命过程。首款靶向RNA的小分子药物利思扑兰(Evrysdi®)的获批打破了传统药物研发对蛋白靶点的依赖,为攻克“不可成药”的靶点提供了新的思路。但行业仍面临着RNA三维结构解析极其昂贵且耗时的“深水区”。
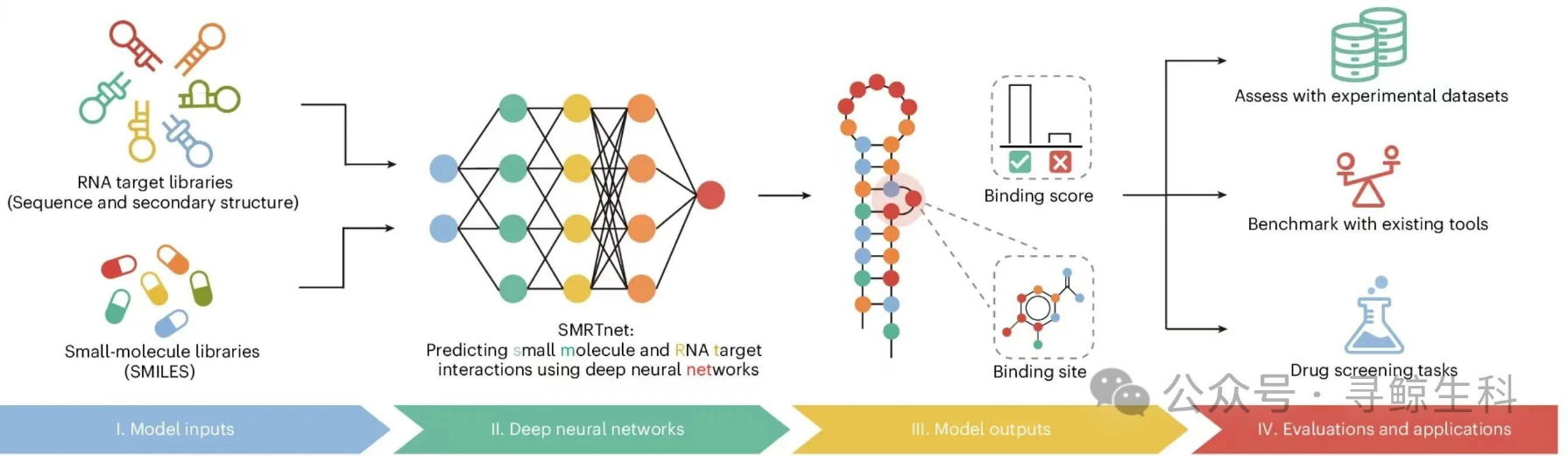
面对传统筛选方法周期长、成功率低的严峻挑战,寻鲸生科创始人团队另辟蹊径,开发了全新的AI方法——SMRTnet。这一突破性的技术无需依赖高难度的RNA三维结构,仅需二级结构信息即可精准预测小分子与RNA的互作关系及其潜在结合位点,极大地拓宽了靶向RNA药物的研发边界。
SMRTnet不仅在理论上实现了跨越,在实测数据中也展现了惊人的表现:
这意味着,我们能够以更快的速度、更低的成本,从海量化合物库中筛选出最具潜力的“种子选手”。
这次科研成果的发表,正是寻鲸生科核心技术平台——SMRT-Mind智能计算平台实力的一个缩影 。
作为国内领先的专注于RNA赛道的人工智能公司,寻鲸生科自成立以来,始终致力于构建“计算+实验”的闭环 :
站在 AI 驱动药物研发的时代风口,寻鲸生科正步入发展的快车道。为进一步加速核心管线向临床阶段迈进,并持续深化 SMRT-Mind 智能计算平台的壁垒优势,公司现已正式启动新一轮融资计划。
本轮募集资金将精准赋能于核心管线的 IND 申报、多模态 RNA 大模型的迭代升级以及全球领先的RNA结构组学数据库的扩充。致力于通过“自主研发+技术赋能”的双轮驱动模式,重塑 RNA 药物研发的效率边界。
※本文转载于“寻鲸生科”公众号,如有侵权请联系删除